La monitorización cerebral multimodal (MMM) permite correlacionar distintos parámetros fisiológicos y metabólicos para detectar precozmente el daño cerebral secundario. Gracias al avance en tecnología, ahora podemos monitorear oxigenación tisular, metabolismo energético, autorregulación vascular y actividad eléctrica cerebral en tiempo real. Esta integración representa un cambio de paradigma en la medicina intensiva neurológica.
En cuidados neurocríticos, la evaluación del paciente va más allá del acrónimo clásico GHOST-CAP (Glucosa, Hemoglobina, Oxigenación, Sedación, Temperatura, Convulsiones, Presión intracraneal). Aunque útil como evaluación inicial, el enfoque moderno exige una visión más profunda y continua del estado cerebral.
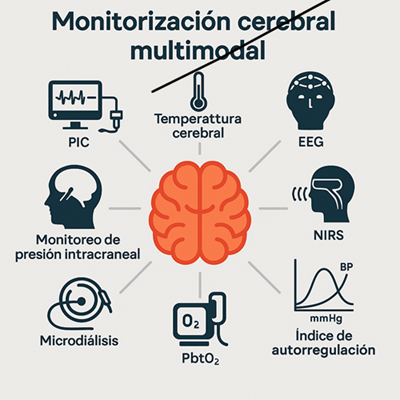
Estrategias y tecnologías recientes
La MMM permite evaluar diversas dimensiones del cerebro lesionado. A continuación, un desglose de las principales herramientas utilizadas actualmente:
1. Monitoreo de presión intracraneal (PIC)
- Indicada en TCE severo, HSA complicada o hidrocefalia aguda.
- Modalidades: catéter intraventricular (gold standard), sensores intraparenquimatosos.
- Límite crítico: PIC >22 mmHg mantenida.
📌 Interpretar junto a PPC, PbtO₂ y metabolismo para evitar decisiones erróneas.
2. Microdiálisis cerebral
- Mide glucosa, lactato, piruvato, glicerol y glutamato.
- Lactato/piruvato >25 sugiere hipoxia o falla mitocondrial.
- Detecta isquemia antes que imagenología o síntomas.
📌 Permite guiar ajustes en ventilación, perfusión y nutrición cerebral.
3. PbtO₂ – Presión parcial de oxígeno en tejido cerebral
- Normal: 20–35 mmHg.
- <15 mmHg: riesgo de hipoxia celular.
- Evalúa oxigenación a nivel local, especialmente sustancia blanca.
📌 Complementa a la PIC y evita tanto hipoxia como sobreoxigenación.
4. Temperatura cerebral directa
- Mide temperatura en el parénquima cerebral, más confiable que central.
- Elevaciones localizadas reflejan inflamación, isquemia o hipertermia neurogénica.
📌 El control térmico agresivo reduce el metabolismo cerebral y protege la función neuronal.
5. EEG continuo (cEEG)
- Detecta crisis subclínicas y actividad epileptiforme.
- Fundamental en coma, post-paro, encefalopatías o HSA.
- Evalúa la respuesta cortical ante sedación.
📌 Hasta el 50% de las crisis en neurocríticos pueden ser no convulsivas.
6. NIRS (Near-Infrared Spectroscopy)
- No invasiva. Se aplica en la frente para medir oxigenación cortical regional.
- Útil en cirugías, sedación profunda, neonatos o entornos sin PIC.
📌 Permite detección temprana de hipoperfusión en entornos limitados.
7. Índice de autorregulación cerebral (PRx, CPPopt)
- PRx evalúa si el cerebro puede autorregular el flujo sanguíneo frente a cambios de presión.
- CPPopt estima la presión de perfusión ideal individual.
📌 Ajustar la PAM según PRx mejora la supervivencia y los desenlaces neurológicos.
8. Imágenes funcionales y perfusionales integradas
Aunque no son monitorización continua, estudios como:
- TC de perfusión
- RM funcional (fMRI)
- PET cerebral
…complementan la evaluación fisiológica con correlatos anatómicos y metabólicos.
✨ Perlas clínicas ampliadas
✅ 1. Un solo parámetro puede engañar. La PIC normal no descarta isquemia; solo el monitoreo integrado revela la situación real.
✅ 2. Detectar a tiempo = prevenir daño irreversible. El deterioro metabólico cerebral suele preceder a los cambios clínicos.
✅ 3. La fiebre no es inocente. Cada grado de temperatura cerebral puede aumentar el metabolismo cerebral en 10%.
✅ 4. El EEG continuo salva vidas. Identifica crisis silenciosas, que son frecuentes y devastadoras si no se tratan.
✅ 5. Personalización real del tratamiento. Gracias al PRx y CPPopt, podemos adaptar hemodinámicamente a cada paciente.
✅ 6. Microdiálisis: el “laboratorio” del cerebro. Permite guiar estrategias metabólicas e identificar disfunción mitocondrial.
✅ 7. NIRS es útil cuando lo invasivo no es opción. Ideal para pacientes pediátricos o en unidades sin neurointensivistas.
✅ 8. Más tecnología ≠ mejor cuidado. La clave es saber cuándo, cómo y por qué integrar cada herramienta.
✅ 9. Tiempo es sinapsis. La detección precoz con MMM cambia el pronóstico funcional a largo plazo.
✅ 10. Se necesita entrenamiento. La interpretación adecuada requiere personal capacitado y protocolos institucionales.
📚 Referencias
- Robba C, et al. Multimodal monitoring of brain physiology: a review of clinical applications and research directions. Critical Care. 2020;24(1):102.
🔗 PubMed Link - Hawryluk GWJ, et al. Management of severe traumatic brain injury: a summary of the Brain Trauma Foundation Guidelines. Lancet Neurol. 2022;21(12):1109–1120.
- Hutchinson PJA, et al. Consensus statement from the International Multidisciplinary Consensus Conference on Multimodality Monitoring in Neurocritical Care. Intensive Care Med. 2014;40(8):1189–1209.



