Se debe sospechar de hipoaldosteronismo en cualquier paciente con hiperkalemia persistente en el que no exista una causa evidente, como insuficiencia renal o el uso de suplementos de potasio o un diurético ahorrador de potasio.
Además de hiperkalemia, el hipoaldosteronismo suele asociarse con una acidosis metabólica leve con un desequilibrio aniónico normal (es decir, una acidosis hiperclorémica) que se ha denominado acidosis tubular renal tipo 4.
Aunque la aldosterona también promueve la retención de sodio, el hipoaldosteronismo no suele asociarse con una pérdida importante de sodio (excepto en niños pequeños) debido a la acción compensatoria de otros factores de retención de sodio (como la angiotensina II y la norepinefrina. La hiponatremia también es poco común en pacientes con deficiencia aislada de aldosterona, ya que no hay estimulación de la liberación de hormona antidiurética (ADH) inducida por la hipovolemia y porque el cortisol plasmático, un inhibidor tónico de la liberación de ADH, es normal.
Cuando hay hiponatremia, debe sospecharse insuficiencia suprarrenal primaria. En este trastorno, la falta concurrente de cortisol es un potente estímulo para la secreción de ADH, lo que conduce a la retención de líquidos y a una caída de la concentración plasmática de sodio.
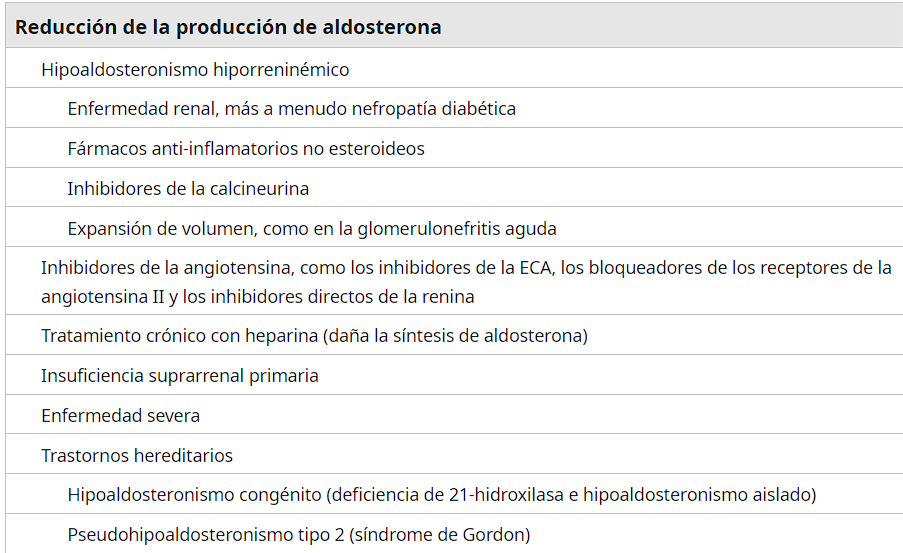
Principales causas de hipoaldosteronismo
Hiperkalemia en hipoaldosteronismo
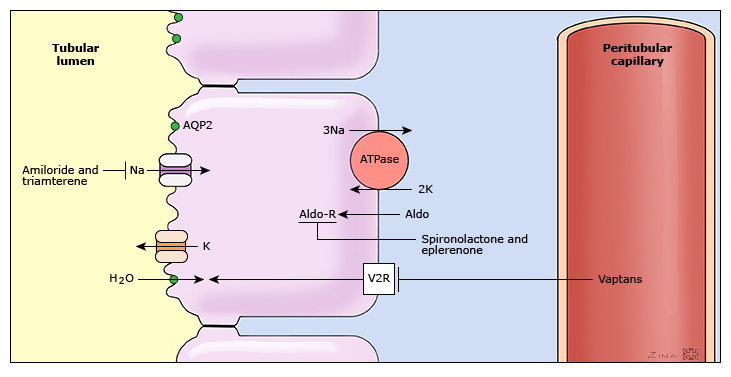
La aldosterona actúa aumentando el número de canales de sodio abiertos en la membrana luminal de las células principales en el túbulo colector cortical, lo que lleva a una mayor reabsorción de sodio. La subsiguiente eliminación de sodio del líquido tubular hace que la luz sea electronegativa, creando así un gradiente eléctrico que favorece la secreción de potasio celular hacia la luz a través de los canales de potasio en la membrana luminal.
La mayoría de los pacientes con hipoaldosteronismo tienen solo una disminución moderada en la liberación o el efecto de la aldosterona, con un pequeño aumento en la concentración plasmática de potasio. El desarrollo de hiperkalemia es más común en pacientes con deficiencia de aldosterona con otros factores de riesgo que deterioran aún más la eficiencia de la excreción de potasio, como deterioro de la función renal, perfusión renal reducida o el uso de medicamentos que interfieren con el manejo del potasio, como la espironolactona, eplerenona, inhibidores de la enzima convertidora de angiotensina, bloqueadores de los receptores de angiotensina II o inhibidores de la renina.
La entrada de sodio filtrado en estas células está mediada por canales de sodio selectivos en la membrana apical (luminal) (ENaC); la energía para este proceso la proporciona el gradiente electroquímico favorable para el sodio (electronegativo en el interior de la celda y baja concentración de sodio en la celda). El sodio reabsorbido es bombeado fuera de la célula por la bomba Na-K-ATPasa en la membrana basolateral (peritubular). La reabsorción de sodio catiónico hace que la luz sea electronegativa, creando así un gradiente favorable para la secreción de potasio hacia la luz a través de los canales de potasio (ROMK y BK) en la membrana apical. Aldosterona (Aldo), después de combinarse con el receptor mineralocorticoide citosólico (Aldo-R), conduce a una mayor reabsorción de sodio y secreción de potasio al aumentar tanto el número de canales de sodio abiertos como el número de bombas de Na-K-ATPasa. Los diuréticos ahorradores de potasio (amilorida y triamtereno) actúan inhibiendo directamente el canal de sodio epitelial; la espironolactona actúa compitiendo con la aldosterona por unirse al receptor de mineralocorticoides.
Acidosis metabólica en hipoaldosteronismo
Generalmente se asocia con una acidosis metabólica leve; la brecha aniónica suele ser normal (es decir, una acidosis hiperclorémica) a menos que haya un deterioro de la función renal concurrente. Esta afección se ha denominado acidosis tubular renal tipo 4 y parece deberse principalmente a la disminución de la excreción urinaria de amonio.
Etiología
Las causas del hipoaldosteronismo incluyen trastornos adquiridos y, con menos frecuencia, hereditarios, que pueden afectar la síntesis de aldosterona suprarrenal o la secreción renal (y quizás suprarrenal) de renina. La actividad de la renina plasmática suele estar aumentada en aquellos trastornos en los que la acción de la aldosterona está disminuida.
Las causas adquiridas más frecuentes de hipoaldosteronismo son el hipoaldosteronismo hiporreninémico, la inhibición farmacológica de la angiotensina II y el tratamiento con heparina. La insuficiencia suprarrenal primaria es una causa infrecuente.
Diagnostico
Los pacientes con sospecha de hipoaldosteronismo deben ser interrogados sobre el uso de cualquier fármaco o la presencia de una enfermedad que pueda alterar la liberación de aldosterona, como un fármaco antiinflamatorio no esteroideo (AINE), un inhibidor de la angiotensina, un inhibidor de la calcineurina, heparina, bloqueadores beta-adrenérgicos , o infección por VIH. Como se discutió anteriormente, otras causas incluyen hipoaldosteronismo hiporreninémico (más a menudo asociado con diabetes y enfermedad renal crónica), insuficiencia suprarrenal primaria, un defecto de la enzima suprarrenal (más a menudo deficiencia de CYP11B2 [aldosterona sintasa, P450c11as]) o los raros trastornos genéticos pseudohipoaldosteronismo tipo 1 y tipo 2.
Las diferentes causas de hipoaldosteronismo se pueden diferenciar mediante la medición de la actividad de la renina plasmática, aldosterona y cortisol séricos. Estas pruebas deben realizarse después de la administración de un diurético de asa o tres horas en posición vertical, lo que aumentará la liberación de renina y aldosterona en pacientes sin hipoaldosteronismo.
Tratamiento
El tratamiento adecuado para el hipoaldosteronismo varía según la causa de la deficiencia hormonal. Los pacientes con insuficiencia suprarrenal primaria, por ejemplo, deben recibir terapia de reemplazo de mineralocorticoides (con fludrocortisona en dosis de 0,05 a 0,2 mg/día) para corregir la hiperpotasemia y con solución salina al 0,9% para corregir la hipovolemia sintomática. La insuficiencia suprarrenal primaria también debe tratarse con un glucocorticoide, como hidrocortisona o prednisona, para corregir la deficiencia de cortisol.
La fludrocortisona también es eficaz en pacientes con hipoaldosteronismo hiporreninémico. La dosis típica requerida para normalizar el potasio sérico es de 0,2 a 1 mg/día, sustancialmente más alta que la dosis en la insuficiencia suprarrenal primaria. Por lo tanto, es probable que estos pacientes tengan algún componente de resistencia a la aldosterona, presumiblemente debido a la enfermedad renal subyacente.
A pesar de su eficacia, la fludrocortisona a menudo no se usa en el hipoaldosteronismo hiporreninémico porque muchos pacientes con este trastorno tienen hipertensión y/o edema, problemas que pueden exacerbarse con el reemplazo de mineralocorticoides. En este contexto, el uso de una dieta baja en potasio y, si es necesario, un diurético de asa o tiazídico generalmente controlará la hiperkalemia.
Fuente
Hypoaldosteronism NCBI
https://www.ncbi.nlm.nih.gov/books/NBK555992/
Enlace interno