En el ámbito hospitalario, la hiperglucemia, tanto en pacientes diabéticos como en los no diabéticos, está asociada a un mayor riesgo de complicaciones, entre las que destaca un claro incremento en la mortalidad.
La hiperglucemia intrahospitalaria se define mediante cifras mayores de 140 mg/dL. Una vez corroborada dicha alteración bioquímica, será preciso identificar el posible origen de la misma: diabetes conocida, diabetes no conocida (sin diagnóstico previo de la enfermedad) o pacientes sin diabetes con hiperglucemia transitoria o de “estrés”.
La hiperglucemia de estrés, o hiperglucemia relacionada con la hospitalización, es una elevación transitoria de la glucosa durante una enfermedad, que puede ser de causa multifactorial: relacionada con el tratamiento hospitalario (glucocorticoides exógenos, nutrición enteral y parenteral), con la respuesta del paciente a la enfermedad (liberación de catecolaminas, de glucagón o activación del eje hipotálamo hipófisis-adrenal) y con la predisposición del paciente (reserva pancreática limitada, resistencia a la insulina).
La hiperglucemia puede ser una manifestación de enfermedad crítica, resultado de un desequilibrio metabólico asociado con una respuesta al estrés. La respuesta predecible a una lesión real o potencial consiste en la liberación de hormonas contrarreguladoras que incrementan la producción hepática de glucosa. Tales cambios tienen como finalidad incrementar el transporte de glucosa hacia tejidos vitales no dependientes de insulina, como lo es el sistema nervioso central, y hacia las células sanguíneas.
Las citocinas proinflamatorias secretadas por estas células afectan indirectamente la homeostasia de la glucosa al facilitar la sobreexpresión de los transportadores GLUT-1 y GLUT-3, lo que permite a ciertos tejidos mayor entrada de glucosa en detrimento de otros, pues, al mismo tiempo, se inhibe el transportador de glucosa dependiente de la insulina (GLUT-4) presente en los tejidos adiposo y muscular. Al mediano plazo esta polarización puede resultar contraproducente debido a glucotoxicidad directa sobre el tejido en cuestión, como se observa en algunas células inmunitarias en las que se altera la quimiotaxis y la fagocitosis. La excesiva glucólisis explica parcialmente tales alteraciones, pues conlleva estrés oxidativo celular.
Abordaje diagnostico
Datos epidemiológicos de Estados Unidos señalan que un tercio de los pacientes hospitalizados tienen hiperglucemia, de los cuales una tercera parte no tenía el diagnóstico previo de diabetes. En tal escenario, la medición de hemoglobina glucosilada puede ayudar a diferenciar a los pacientes diabéticos no conocidos, con un valor superior a 6.5%, de aquellos con hiperglucemia de estrés.
El grado de la hiperglucemia de estrés guarda una correlación positiva con la gravedad de la respuesta inflamatoria sistémica. Durante la enfermedad crítica, por tanto, es obligada la determinación de la glucemia.
Tratamiento hiperglucemia en pacientes hospitalizados
Es preciso establecer metas de tratamiento ante la hiperglucemia, evitando a toda costa la hipoglucemia (< 70 mg/dL). La meta es mantener una glucosa en ayuno y preprandial inferior a 140 mg/dL y una glucosa al azar inferior a 180 mg/dL. Por otro lado, se puede considerar el mantenimiento de niveles más altos de glucosa en pacientes terminales y muy ancianos o cuando el monitoreo sea deficiente para evitar hipoglucemias. En el paciente hospitalizado con hiperglucemia la insulina es el medicamento de elección en todas las situaciones. Fuera de la unidad de terapia intensiva, la insulina subcutánea es el método preferido para el control de la hiperglucemia. La administración exógena de insulina es capaz de revertir la resistencia periférica mediada por la inhibición de los transportadores GLUT-4, además, atenúa el hipercatabolismo tanto proteico como graso, y ayuda a revertir la disfunción endotelial y la hipercoagulabilidad en los estados sépticos.
Hiperglucemia en el paciente con diabetes mellitus tipo 2
El régimen de insulina subcutánea ideal debe consistir en un componente basal y otro de corrección prepandial. Dado lo erráticas que pueden ser la ingestión y la absorción de alimentos en un paciente enfermo, el retiro de los hipoglucemiantes orales y de los bolos prepandiales de insulina puede disminuir el número de eventos de hipoglucemia, lo cual constituye una meta de suma importancia en la calidad de atención hospitalaria.
La dosis total diaria de insulina basal a administrar debe calcularse de acuerdo con los siguientes principios: (Solo recomendación para fines prácticos, deberá ajustarse en base en base al contexto del paciente)
- 0.3 unidades/kg/día si el paciente tiene más de 70 años de edad o la tasa de filtrado glomerular es inferior a 60 mL.
- 0.4 unidades/kg/día si la glucosa en el momento del ingreso va de 140 a 200 mg/dL.
- 0.5 unidades/kg/día si la glucosa en el momento del ingreso va de 201 a 400 mg/dL.
Entre las insulinas basales, la insulina NPH es la de menor coste. Sin embargo, para una verdadera cobertura basal esta insulina debe administrarse dos veces por día, dividiendo la dosis en tres partes iguales: dos tercios de la dosis calculada se administra a las 8 am y el tercio restante a las 10 pm. Su mayor desventaja es su pico máximo de acción en el que puede sobrevenir un descenso brusco de glucosa.
Las insulinas de acción prolongada (p. ej., glargina) se aplican en una dosis única por día (vida media aproximada de 24 h). Existe un menor riesgo de hipoglucemia con el uso de estas insulinas debido a que están exentas de pico (momento en el que la insulina logra su máximo efecto).
La insulina de corrección se administra de forma prepandial, y puede ser individualizada utilizando 5% de la dosis total diaria de insulina calculada; por ejemplo, si el paciente requiere una dosis de insulina de 60, entonces 5% de la dosis es tres unidades, por lo que la escala se diseña con incrementos de tres en tres: > 141 a 180 = 3 unidades; 181 a 220 = 6 unidades; 221 a 260 = 9 unidades; y 261 a 300 = 12 unidades. Lo más sencillo, no obstante, es aplicar un esquema basado en esquemas prefijados de sensibilidad de insulina.
Si el paciente requiere ayuno se debe suspender la insulina basal y dejar la insulina de corrección cada seis horas a “sensible a la insulina”.
Hiperglucemia en el paciente con diabetes mellitus tipo 1
El régimen externo de insulina de un paciente dado puede no ser apropiado en el hospital. Sin embargo, y aún en ayuno estricto, los pacientes con diabetes mellitus tipo 1 requieren siempre de cobertura con insulina basal, además de la insulina de corrección. En ellos la dosis total diaria de insulina basal a administrar es de 0.3 unidades/kg/día. Otra opción es utilizar el 50% de la dosis basal utilizada en casa.
Hiperglucemia de estrés
En los pacientes no diabéticos con riesgo de hiperglucemia relacionada con el hospital (uso de glucocorticoides exógenos, nutrición parenteral) se debe hacer un monitoreo de la glucosa en las primeras 24 a 48 h. Si la glucosa se mantiene < 140 mg/dL durante este periodo, se puede suspender el monitoreo, pero si es > 180 mg/dL se debe manejar con insulina. En la hiperglucemia por uso de nutrición parenteral (NPT) se debe monitorear la glucosa capilar cada seis horas y el manejo debe ser en conjunto con el equipo de nutrición clínica, debido a la cantidad de insulina que viene preañadida en la bolsa. Se puede agregar insulina basal y corregir de acuerdo a las necesidades. En la hiperglucemia por nutrición enteral, si ocurrió por alimentación continua, se monitorea la glucosa capilar cada seis horas y se emplea insulina de corrección; en la alimentación en bolos se puede utilizar insulina en bolo preprandial. En la hiperglucemia por uso de glucocorticoides se recomienda la insulina basal en dosis de 0.3 a 0.5 u/kg/día. Al disminuirse la dosis del esteroide se debe reducir también la dosis de insulina, para evitar hipoglucemias.
Ajustes
El monitoreo de la glucometría para los ajustes debe ser en ayuno y prepandial. Si el paciente desarrolla hipoglucemia en ayuno se debe disminuir la insulina basal a 20%. Si el paciente persiste con hiperglucemia en ayuno se aumenta la insulina basal a 10% si la glucosa es > 140 mg/dL y a 20% si es > 180 mg/ dL. El ajuste de la insulina basal puede también basarse en la dosis total de la corrección del día previo: se añade 50% de las unidades requeridas de la corrección a la basal.
Transición al manejo ambulatorio
Es necesario conocer el nivel de hemoglobina glucosilada (HbA1c) del enfermo, así como el tiempo de diagnóstico de la diabetes y la existencia de apoyo familiar para planear el tratamiento antidiabético ambulatorio. Será necesario explicar al paciente y los familiares las metas de control glucémico que deben cumplirse:
- Glucemia plasmática en ayunas inferior a 130 mg/dL.
- Hemoglobina glucosilada inferior a 7%.
- Glucemia postprandial inferior a 180 mg/dL (medida 2 h después del primer bocado).
Las dosis y la frecuencia de los medicamentos deber ser explicada y entregada por escrito. Siempre es prudente, además, instruir sobre los datos de hipoglucemia y las medidas para actuar en consecuencia. Los pacientes con diabetes mellitus tipo 2 y HbA1c muy por encima de la meta (> 8%) deben ser egresados con insulina basal (NPH o glargina) y metformina, a menos que tengan alguna contraindicación para el uso de biguanidas (fallar renal o hepática).
El mecanismo de acción de la metformina implica varias vías metabólicas:
- Reduce la producción hepática de glucosa
- Aumenta la sensibilidad a la insulina
- Disminuye las concentraciones del factor 1 de crecimiento similar a la insulina (IGF1)
- Inhibe la lipogénesis
- Disminuye el estrés oxidativo
- Tiene un efecto inhibidor del crecimiento celular en el cáncer.
Además de metformina 850 cada 8 a 12 h (máximo de 2 550 mg/día). Si el nivel de HbA1c al momento de la hospitalización está dentro del rango de control se continúa con la misma terapéutica antidiabética que llevaba previo a su ingreso.
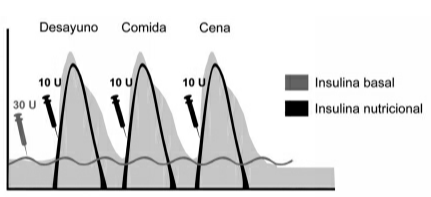
Todos los pacientes con diabetes mellitus tipo 1 precisan de monoterapia con insulina basal más bolo nutricional en cada alimento; en tales casos la dosis total diaria de inicio es de 0.3 unidades/kg/día. La dosis total resultante se divide en dos mitades y se reparte entre el componente basal y el nutricional (el 50% al componente basal y el 50% restante al componente nutricional). Por ejemplo, supongamos que tenemos un paciente con una dosis total diaria de insulina de 60 unidades: 30 unidades deben ser inyectadas en la forma de insulina basal y 30 unidades en la forma de insulina nutricional. Ahora bien, la insulina nutricional debe administrarse para contrarrestar la elevación drástica de la glucosa tras los alimentos, de modo que el paciente debe inyectarse 10 unidades con el desayuno, 10 con la comida y 10 con la cena (que sumaron las 30 unidades de la insulina nutricional).
Para los ajustes de la insulina nutricional se utiliza un ajuste con base en la glucemia postprandial. Si la glucosa postprandial es mayor a 180 mg/dL, se aumenta la dosis de insulina en 2 unidades cada tercer día hasta conseguir la meta. Los ajustes de la insulina basal precisan de la medición de la glucemia plasmática en ayunas. Si la glucosa en ayuno no está en los rangos deseados (70-130 mg/dL) al día tres de la terapia, la dosis de la insulina basal se aumenta en 2 unidades cuando la glucosa en ayuno está relativamente cerca de la meta (p. ej., 130-180 mg/dL). Ahora bien, si la glucosa está muy por encima de los rangos (> 180 mg/dL) se debe aumentar la insulina basal a razón de 4 unidades con ajustes similares cada tercer día.
Manejo de la hiperglucemia en el área de urgencias
Algunos pacientes pueden acudir al servicio de urgencias con diabetes manifiesta (poliuria, polidipsia, polifagia, pérdida de peso y debilidad secundaria a la pobre utilización de la glucosa) que, sin embargo, no cumplen el criterio de una complicación aguda de la diabetes (cetoacidosis diabética o estado hiperosmolar hiperglucémico).
El cribado más conveniente consiste en realizar tira reactiva de orina para descartar cetonuria en todo paciente que se presente con hiperglucemia marcada (superior a 250 mg/dL). Las cetonas negativas en orina (tira reactiva) descartan la cetoacidosis diabética con 100% de valor predictivo negativo.10 La hiperglucemia sin complicación aguda no requiere internamiento, solo observación por un par de horas. La deshidratación secundaria a la poliuria puede ameritar hidratación con suero salino a 0.9% (1 L para 1-2 h). Además, es prudente aplicar insulina regular ante valores de glucemia superiores a 300 mg/dL. Pacientes con glucemia en un nivel inferior no requieren manejo agudo con insulina. La insulina se aplica por vía subcutánea a razón de 0.1 unidad/kg, con determinación de la glucemia 1-2 h después. La dosis de insulina puede repetirse si la glucosa no disminuye en el orden de 50 mg/dL. El paciente puede ser egresado ante cifras de glucemia inferiores a 250 mg/dL, siempre y cuando se encuentre bien hidratado.
Es importante establecer si hubo trasgresión dietética o terapéutica para actuar en consecuencia. La dieta, la actividad física y el manejo farmacológico son los tres pilares en el tratamiento de la diabetes mellitus; los dos primeros entrañan dificultad y complejidad al involucrar aspectos culturales y sociales. Las causas más comunes de descontrol glucémico son la constante transgresión dietética y la falta de apego al tratamiento. Por ello, es importante involucrarse en el estado afectivo del paciente diabético para guiarlo hacia el autocuidado.
Enlace interno
Medicina interna » Medical & Gabeents
Enlace externo
Practice Guidelines Resources | American Diabetes Association




[…] niveles altos de glucemia se relacionan con un mal pronóstico, El control adecuado de la misma disminuye la estadía en la UCI, las infecciones, las polineuropatías y la […]
[…] La glucosa es la principal fuente de energía de la neurona. La hipoglucemia (≤ 80 mg/dL) puede afectar el metabolismo cerebral y la hiperglucemia (≥ 180 mg/dL) también se ha asociado con peores resultados. En pacientes con lesión cerebral aguda, el control estricto de la glucemia puede no mejorar significativamente los resultados y puede aumentar el riesgo de hipoglucemia. Los niveles objetivo entre 80 y 180 mg/dL son adecuados. […]