Los pacientes críticamente enfermos pueden experimentar dolor debido a una enfermedad o lesión subyacente, cirugía reciente o estímulos nocivos. La subestimación y el tratamiento insuficiente del dolor son comunes en este entorno.
La lesión tisular conduce a la liberación de mediadores inflamatorios con la posterior estimulación de los nociceptores. Los impulsos de dolor se transmiten al asta dorsal de la médula espinal, donde hacen contacto con neuronas de segundo orden que cruzan al lado opuesto de la médula y ascienden a través del tracto espinotalámico al sistema de activación reticular (RAS) y al tálamo. La localización y el significado del dolor ocurre a nivel de la corteza somatosensorial.
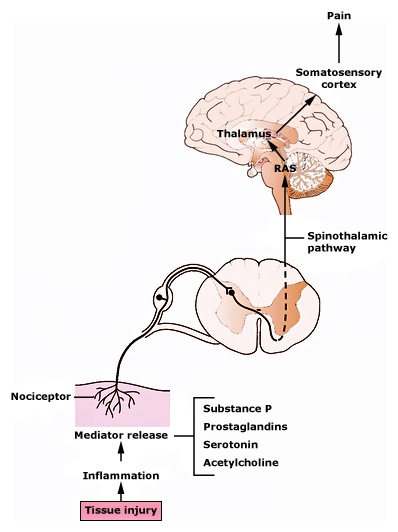
La imagen ilustra el proceso de transmisión del dolor desde una lesión en los tejidos hasta el cerebro. En la parte inferior, se muestra una lesión en el tejido que activa los nociceptores, los cuales detectan el daño y liberan mediadores como la sustancia P, prostaglandinas, serotonina y acetilcolina. Estos mediadores provocan inflamación y generan una señal de dolor.
La señal se transmite a través de una vía llamada espinotalámica que asciende por la médula espinal y llega al tálamo, donde se integra y se envía al córtex somatosensorial. El sistema de activación reticular (RAS) también participa en la modulación de la percepción del dolor.Evaluación del dolor
El mantenimiento de un nivel individualizado aceptable de comodidad requiere evaluaciones de dolor frecuentes de rutina que documenten la gravedad, la respuesta a la medicación y el desarrollo de efectos secundarios.
- Pacientes que pueden comunicarse
Para los pacientes que pueden comunicarse, utilizamos un análogo visual o una escala de dolor de calificación numérica.
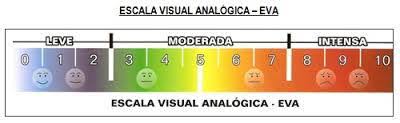
La imagen muestra una Escala Visual Analógica (EVA) para la evaluación del dolor, que ayuda a medir la intensidad del dolor que experimenta un paciente. La escala está dividida en tres categorías de dolor:
Leve (0-3), representado en tonos de azul y verde, indica una molestia mínima.
Moderada (4-6), representada en tonos amarillos y verdes, indica un dolor que empieza a ser significativo.
Intensa (7-10), representada en tonos naranjas y rojos, indica un dolor severo.
Cada nivel tiene una puntuación del 0 al 10, donde 0 representa "sin dolor" y 10 representa "el peor dolor posible", acompañado de expresiones faciales que van desde una sonrisa hasta una mueca de dolor.- Pacientes que no pueden comunicarse
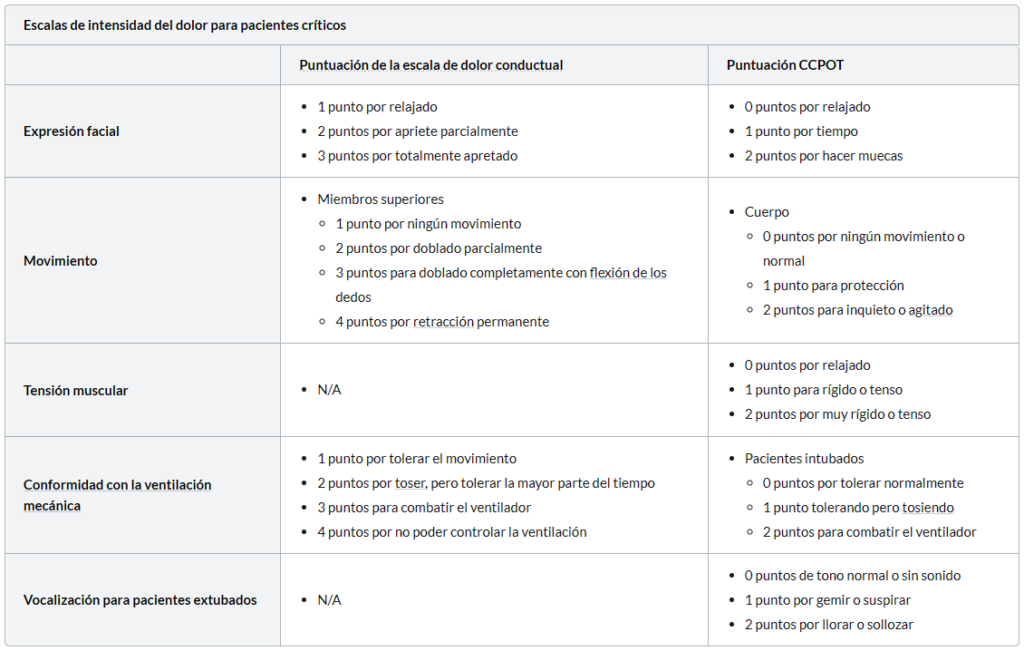
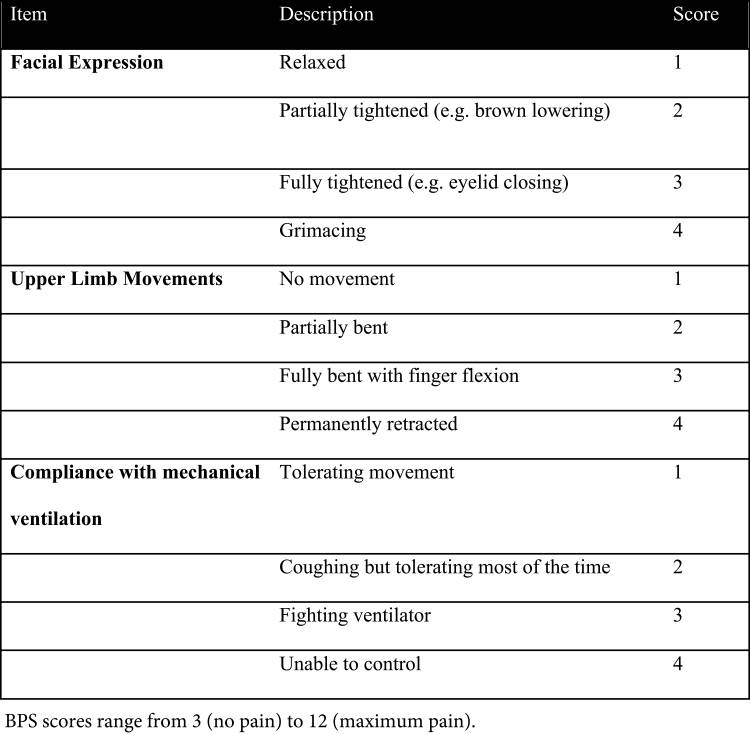
Para los pacientes que no pueden comunicarse, utilizamos una herramienta validada de calificación del dolor con comportamientos relacionados con el dolor e indicadores fisiológicos (por ejemplo, Escala de dolor conductual o Herramienta de observación del dolor de cuidados críticos)
- Objetivos del adecuado manejo del dolor
Los objetivos del control del dolor son:
- Proporcionar una comodidad óptima al paciente
- Atenuar las respuestas fisiológicas adversas al dolor
- Prevenir el desarrollo de síndromes de dolor crónico
- Controlar la ansiedad y el delirio
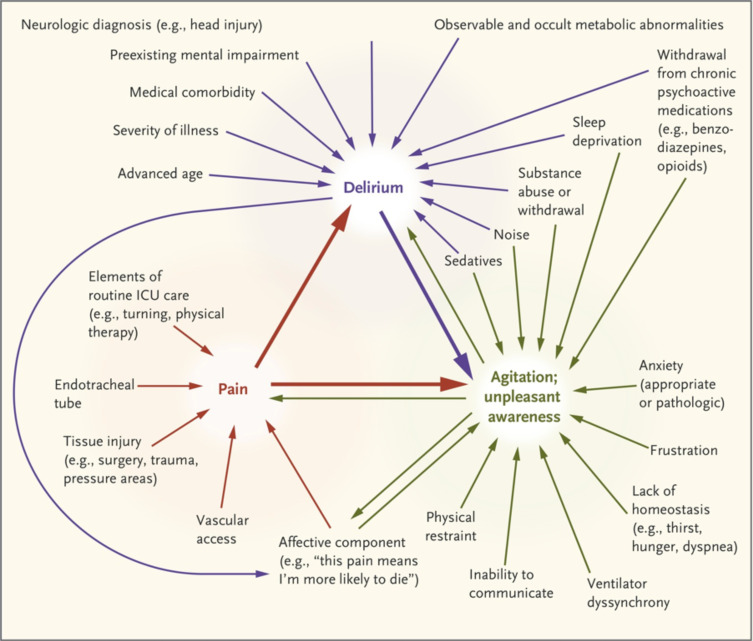
La imagen es un diagrama que representa los factores interrelacionados de delirio, agitación y dolor en pacientes de cuidados intensivos (UCI). Muestra cómo estos tres estados están interconectados y se ven influenciados por diversos factores clínicos y ambientales en el entorno de la UCI.
Desglose de los factores
Delirio: Factores como la edad avanzada, enfermedades neurológicas, comorbilidades, gravedad de la enfermedad, alteraciones metabólicas, abuso de sustancias, privación de sueño y el uso de sedantes contribuyen al desarrollo del delirio.
Agitación / Conciencia Desagradable: Se relaciona con factores como la ansiedad, frustración, falta de homeostasis (sed, hambre, disnea), disincronía con el ventilador, restricciones físicas, incapacidad de comunicación y abstinencia de medicamentos psicoactivos.
Dolor: Puede ser causado por procedimientos invasivos, lesiones de los tejidos (cirugía, trauma), acceso vascular, la intubación y los elementos de cuidado rutinario de la UCI (como movilización y terapia física). Además, el componente afectivo del dolor influye en la percepción de amenaza y empeora la experiencia de dolor.
Las flechas indican cómo estos tres estados se influyen mutuamente, creando un ciclo en el que el dolor puede llevar a agitación, la agitación puede inducir delirio, y el delirio puede incrementar la percepción de dolor y agitación.Manejo del dolor en pacientes críticos
- Analgésicos opioides: los opioides intravenosos se utilizan como tratamiento de primera línea del dolor no neuropático para la mayoría de los pacientes críticamente enfermos, incluidos aquellos que tienen ventilación mecánica.
- Ventilación mecánica: para el dolor y / o la angustia en pacientes que reciben ventilación mecánica, se prefiere el fentanilo, morfina o hidromorfona porque estos agentes son de acción rápida y titulables. Si se anticipa una extubación temprana, se puede seleccionar remifentanilo debido a su duración de acción ultracorta.
- Dolor no neuropático de moderado a severo: para el dolor no neuropático de moderado a severo en pacientes extubados, preferimos fentanilo intravenoso, morfina o hidromorfona porque estos agentes generalmente se pueden ajustar para lograr una analgesia satisfactoria sin causar depresión respiratoria severa.
- Insuficiencia renal y/o hepática: para pacientes con insuficiencia renal y/o hepática, normalmente seleccionamos fentanilo o hidromorfona IV, con ajustes de dosis según sea necesario. En pacientes con insuficiencia multiorgánica grave, se puede seleccionar remifentanilo porque su metabolismo no depende de la función hepática o renal.
- Inestabilidad hemodinámica: para los pacientes con inestabilidad hemodinámica, preferimos el fentanilo o el remifentanilo porque estos agentes son de acción corta y liberan poca histamina.
- Broncoespasmo agudo: para los pacientes con broncoespasmo agudo, preferimos agentes que liberan poca histamina (por ejemplo, fentanilo, remifentanilo o hidromorfona) en lugar de morfina.
- Necesidad de evaluaciones neurológicas frecuentes: para los pacientes que requieren evaluaciones neurológicas frecuentes, preferimos el remifentanilo debido a su duración de acción ultracorta, lo que permite una reversión rápida para cada evaluación.
- Necesidad de bolos intermitentes: para los pacientes que solo requieren dosis intermitentes de opioides en bolo, preferimos morfina o hidromorfona debido a sus duraciones de acción más largas en comparación con el fentanilo.
Si se desea la administración oral o enteral, generalmente seleccionamos opiáceos orales de acción prolongada (p. ej., metadona, oxicodona de liberación prolongada, sulfato de morfina de liberación prolongada). El fentanilo transdérmico puede beneficiar a los pacientes hemodinámicamente estables con necesidades analgésicas crónicas, aunque hay un retraso de 12 a 24 horas hasta el efecto máximo.
Elección del tratamiento
La dosificación de opioides puede reducirse o eliminarse mediante el uso de uno o más analgésicos no opioides IV. La selección depende del tipo de dolor (no neuropático versus neuropático), la gravedad del dolor, el grado deseado de sedación versus vigilia y los posibles efectos adversos de los agentes.
Enfoque multimodal: un enfoque multimodal para el control del dolor incluye una combinación de analgésicos opioides y no opioides, bloqueos nerviosos neuroaxiales o periféricos, tratamientos no farmacológicos y / o agentes sedantes. Las ventajas de este enfoque incluyen una mejor analgesia, dosis más bajas de opioides y un menor riesgo de efectos secundarios relacionados con los opioides o el desarrollo de tolerancia, abstinencia o hiperalgesia inducida por opioides.
Referencia
Clinical Guidelines – AAPM (painmed.org)
Analgesia for the critically ill patient – EMCrit Project





[…] El control del dolor es clave en el manejo del paciente en UCI, ya que el mismo impacta negativamente en la recuperación fisiológica y psicológica del paciente (ej: en el paciente neuro crítico los episodios de dolor aumentan significativamente la presión intracraneal). Uno de los grandes mitos es creer que aquellos pacientes que están sedados no experimentan dolor. Los pacientes en UCI experimentan dolor por la propia patología y también por los procedimientos de rutina que reciben (rotación, cambio de apósitos, aspiraciones, etc.). […]
[…] comodidad del paciente, incluido el control del dolor, la agitación, la ansiedad y los escalofríos, es un objetivo importante para evitar el […]