El término «infarto cerebral maligno» fue utilizado por primera vez para caracterizar el infarto completo del territorio de la arteria cerebral media acompañado de un efecto de masa que ocupa espacio que se desarrolla durante los primeros 5 días después de la presentación y que se asocia con aproximadamente el 80% de mortalidad.
La RM o TC de perfusión es superior para definir el tamaño del infarto y predecir la evolución maligna. La resonancia magnética en difusión ayuda a la predicción de la evolución maligna tan pronto como 6 h después del inicio de los síntomas, con alta especificidad y un alto valor predictivo positivo y negativo.
Un volumen de cerebro afectado en resonancia magnética de difusión por encima de 82 ml fue el predictor más potente de la evolución maligna, con una alta especificidad (0,98) pero más bien baja sensibilidad.
Menos del 10 % de los accidentes cerebrovasculares isquémicos se clasifican como malignos debido al edema cerebral que ocupa espacio. Las características clínicas de un gran infarto hemisférico en riesgo de edema cerebral con efecto de masa generalmente incluyen desviación de la mirada, déficit del campo visual, hemiplejia y afasia, dependiendo del hemisferio involucrado. La etiología de la mayoría de estos infartos es la oclusión cardioembólica o trombótica de la arteria carótida interna o del segmento proximal de la arteria cerebral media. La mortalidad es tan alta como el 78 % debido a la hernia del lóbulo temporal en el tronco encefálico.
Los marcadores que pueden predecir el edema maligno después de un gran infarto hemisférico incluyen el desarrollo temprano de disminución de la conciencia, edad temprana (< 50 años), puntuaciones más altas de la Escala nacional de accidentes cerebrovasculares de los Institutos Nacionales de Salud (NIHSS) al ingreso y evidencia de infarto temprano que involucra al > 50 % el territorio de la arteria cerebral media en tomografía o la resonancia magnética (IRM).
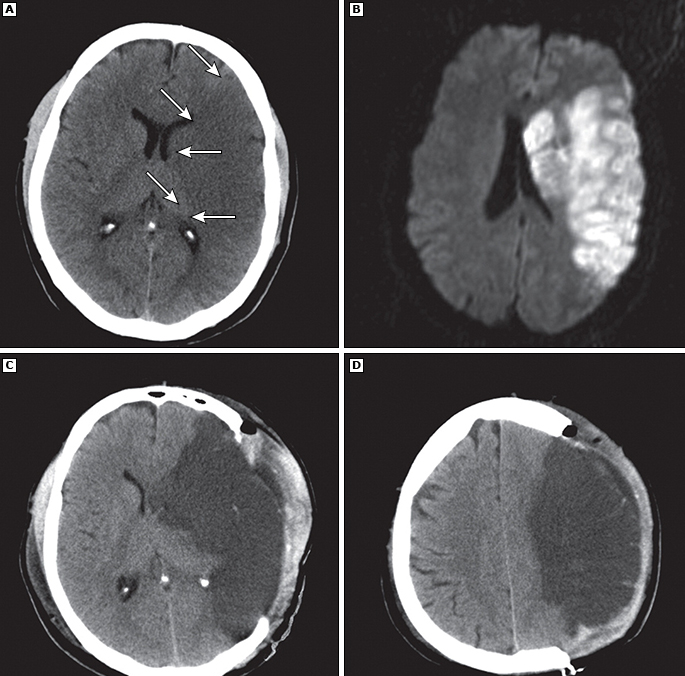
(B) Resonancia magnética ponderada por difusión axial en la fase aguda del infarto maligno de MCA.
(C) y (D) TC axial en el segundo día después del inicio de los síntomas después de la hemicranectomía. Tenga en cuenta que a pesar de la cirugía descompresiva, es evidente una compresión del sistema ventricular con un ligero desplazamiento de la línea media (C; TC axial a nivel de los ganglios basales) y una hinchazón inicial hacia afuera (D; TC axial a nivel supraventricular) del tejido cerebral isquémico.
Tratamiento
Tanto el manitol como la solución salina hipertónica son opciones de tratamiento médico de primera línea para el edema cerebral, pero sorprendentemente se han realizado pocos ensayos clínicos para estudiar su impacto en el resultado clínico.
Los pacientes que presentan signos y síntomas de efecto de masa, como disminución del nivel de excitación o náuseas y vómitos, son candidatos apropiados para la osmoterapia. En tales casos, el uso de la osmoterapia debe provocar una reevaluación del volumen del infarto mediante neuroimagen, ya sea por tomografía computarizada o resonancia magnética.
Manitol
La administración de manitol en el contexto del edema cerebral sintomático debe basarse en el peso: 1 gr / kg por vía intravenosa, repetirse cada 4 a 6 h.
Debido a que el manitol actúa como un diurético, las principales complicaciones incluyen hipovolemia e hipotensión. Los objetivos estrictos de fluidos y el reemplazo de volumen son esenciales. El aclaramiento deficiente de manitol puede manifestarse como nefrotoxicidad. La práctica común incluye repetir las mediciones de la osmolaridad sérica y retener las dosis repetidas de manitol cuando la osmolaridad excede los 320 mOsm.
Solución salina hipertónica
Evita el efecto diurético del manitol y también es eficaz para reducir el edema. Se utilizan clínicamente varias concentraciones, hasta bolos de 30 ml de solución salina al 23,4%. Los aumentos rápidos de sodio en este contexto no parecen causar otras complicaciones neurológicas que uno pueda temer con los grandes aumentos de sodio observados con la rápida corrección de la hiponatremia.
Los niveles de sodio de hasta 160 mmol / L pueden ser aceptables, más allá de lo cual la hipernatremia persistente puede provocar un empeoramiento del delirio, convulsiones y un mal resultado general.
Otros tratamientos
Esteroides
No se recomienda su uso, se han evaluado en varios tipos de lesión cerebral, incluido el infarto cerebral. No se ha encontrado ningún beneficio en el uso de corticosteroides en el accidente cerebrovascular isquémico (o hemorragia intracerebral).
Barbitúricos
Son efectivos para reducir la PIC al reducir la tasa metabólica cerebral, y pueden tener cualidades neuroprotectoras como eliminadores de radicales libres. Sin embargo, el uso de barbitúricos a menudo se complica por hipotensión y sedación. Se pierde la capacidad de seguir el examen neurológico.
Hiperventilación
Reduce la PIC al reducir el volumen sanguíneo cerebral. El dióxido de carbono es un potente vasodilatador cerebral, por lo que la vasoconstricción es inducida por la disminución de pCO2. El efecto es casi inmediato, reduciendo la PIC típicamente en cuestión de minutos. Sin embargo, el efecto es de corta duración. Existe el riesgo de vasodilatación de rebote y empeoramiento de la PIC cuando la pCO2 vuelve a la normalidad. La hiperventilación debe utilizarse como medida temporizadora mientras se espera un tratamiento definitivo para un paciente con hernia aguda.
Temperatura
La modulación de la temperatura es una consideración importante. Se ha encontrado que el aumento de la temperatura corporal está fuertemente asociado con una mayor duración de la UCI y la estancia hospitalaria, así como una mayor mortalidad y un peor resultado. Mantener la normotermia es un objetivo razonable. No se ha determinado la duración óptima de la hipotermia inducida y la incidencia de posibles complicaciones como infección, arritmias y coagulopatía. En la actualidad, la hipotermia inducida sigue siendo en fase de investigación.
Monitorización de la PIC
No hay evidencia de apoyo de que la monitorización de la PIC mejore el resultado o facilite el tratamiento médico. A pesar de esta limitación, la mayoría de los tratamientos están dirigidos a los signos directos o indirectos de la PIC elevada.
Craniectomía descompresiva
Edad. Bajo las circunstancias apropiadas, los pacientes de 60 años o menos deben ser fuertemente considerados para CD, ya que el resultado puede mejorarse. Los pacientes mayores de 60 años también pueden ser considerados, ya que la mortalidad puede mejorar, pero los resultados son generalmente menos favorables.
Variables a tener en cuenta
Tamaño del infarto: Los ensayos en los que la DC demostró beneficio incluyeron pacientes con volúmenes de infarto muy grandes. Un umbral de 145 ml o más tiene la sensibilidad máxima reportada (100%) y la especificidad (94%).
Hemisferio: Si el hemisferio involucrado es dominante o no dominante a veces se considera un factor importante en la toma de decisiones con respecto a la DC. Sin embargo, la evidencia anecdótica sugiere que al menos algunos pacientes con afectación del hemisferio dominante están contentos de haber salvado sus vidas.
La hemicraniectomía para el infarto hemisférico maligno reduce sustancialmente la mortalidad. Sin embargo, la mayoría de los pacientes sobrevivientes quedan con una discapacidad importante. Por lo tanto, el dilema para los pacientes y las familias es que la cirugía puede dejar a los pacientes vivos con discapacidad grave, mientras que el manejo médico solo con mayor frecuencia resulta en la muerte.
Para los pacientes de 60 años o menos con infarto que involucra >50 por ciento del territorio de MCA asociado con un nivel disminuido de conciencia, que por lo tanto tienen un alto riesgo de desarrollar edema maligno, pueden ser candidatos para hemicraniectomía descompresiva (DHC) si la cirugía se puede iniciar dentro de las 48 horas posteriores al inicio del accidente cerebrovascular.
Las posibles complicaciones incluyen hidrocefalia, infecciones, convulsiones, hemorragia intracraneal y acumulaciones de líquidos, síndrome de colgajo de piel que se hunde y hernia paradójica. (Consulte ‘Complicaciones’ más arriba).
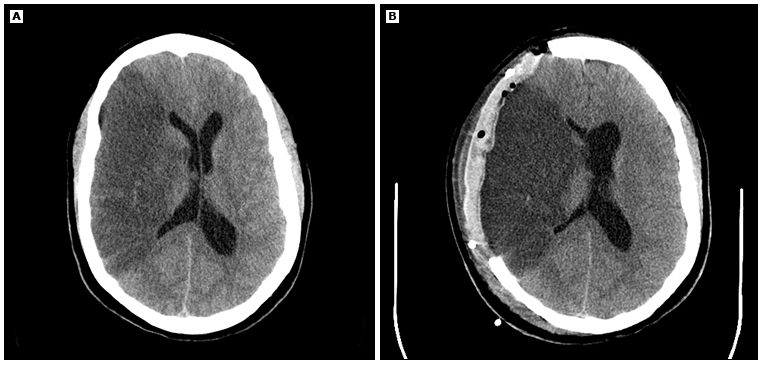
(Panel B) Tomografía computarizada de la cabeza después de la hemicranectomía descompresiva.
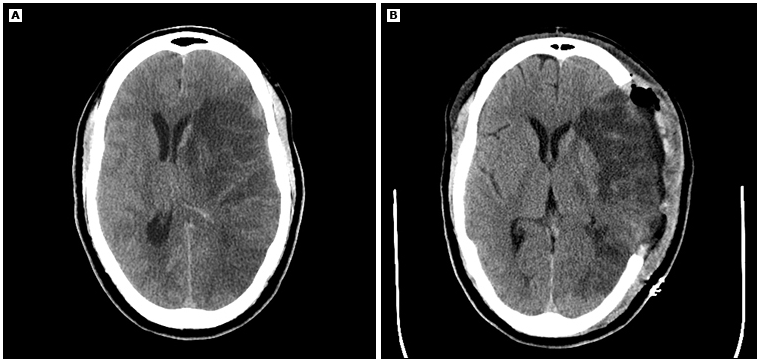
(Panel B) Tomografía computarizada de la cabeza después de la hemicranectomía descompresiva.
Otras medidas
Para todos los pacientes: elevación de la cabecera del lecho de 30 grados y líquidos intravenosos para mantener la euvolemia.
Si el paciente está inconsciente, intubación y ventilación mecánica, con el objetivo de mantener la eucarbia (pCO2, 35–40 mm Hg). Usar hiperventilación (pCO)2, 25–35 mm Hg) sólo en el contexto de la hernia transtentorial; debe limitarse a 30 minutos o menos «en el camino hacia el quirófano».
Aproximadamente a las 36 h, se obtiene un «TC de referencia» y un «examen de referencia», idealmente, tratamiento individualizado.
Referencias
Cerebral Edema Associated With Large Hemispheric Infarction
Implications for Diagnosis and Treatment
David S. Liebeskind, Eric Jüttler, Yuriy Shapovalov, Ashley Yegin, Jaren Landen and Edward C. Jauch
Originally published20 Aug 2019 | https://doi.org/10.1161/STROKEAHA.118.024766 | Stroke. 2019;50:2619–262
Prediction of Malignant Middle Cerebral Artery Infarction Using Computed Tomography-Based Intracranial Volume Reserve Measurements
Jens Minnerup, Heike Wersching, E. Bernd Ringelstein, Walter Heindel, Thomas Niederstadt, Matthias Schilling, Wolf-Rüdiger Schäbitz and André Kemmling
Originally published8 Sep 2011 | https://doi.org/10.1161/STROKEAHA.111.619734 | Stroke. 2011;42:3403–3409



